 产业资讯
产业资讯
 中国医药创新促进会
中国医药创新促进会  2023-11-14
2023-11-14
 1786
1786
11月11日,在南京举办中国药科大学国家药物政策与医药产业经济研究中心(简称NDPE)十周年学术年会上,中国医药创新促进会执行会长、NDPE执行副主任宋瑞霖分享了“新形势下的中国医药创新”的主题报告。宋会长在报告中从医药创新的国际形势为出发点,分析三医协同发展的新形势和当前面临的挑战,为我国源头创新的发展提出了建议。

宋会长指出当下医药行业的国际形势迈入新阶段,一方面全球生物医药行业投资热度下降、行业增长放缓,世界各国均选择通过制度改革或政策激励机制进一步挖掘生物医药产业潜力,如美国开始启动《国家生物技术和生物制造计划》,以促进美国生物技术创新、提升生物制造能力,欧盟委员会也于今年公布了欧盟药品立法修订提案,其关键目标是减少整个欧洲在新药可及性方面的差异;另一方面,对于制约科技发展的外部环境如国际上的技术封锁、人才限制、产业打压等日益增多,中国亟需改善和优化可持续创新的生态环境,提高科技自立自强和创新能力。
11月8日习总书记在2023年世界互联网大会乌镇峰会开幕式上表示“当今世界变乱交织,百年变局加速演进,如何解决发展赤字、破解安全困境、加强文明互鉴,是我们共同面临的时代课题”。创新驱动是我国的国策,在新的国际形势下,中国更需思考如何通过政策的进一步改革完善三医协同治理,从而推动中国真正从“制药大国”走向“制药强国”。
药品监管:进一步提升监管能力与国际化水平
宋会长指出,自2017年加入ICH之后,我国医药创新研发标准逐步与国际全面接轨,在5年内将ICH指导原则落地转化率提升至100%;与此同时,今年11月国家药监局正式申请加入PIC/S,开起了中国医药从临床试验到质量监管全链条的国际接轨。同时,中国新药研发数据质量已经经受住全球考验,2015至2021年 FDA 对中国进行生物研究检查(BIMO)的通过比例达到100%。

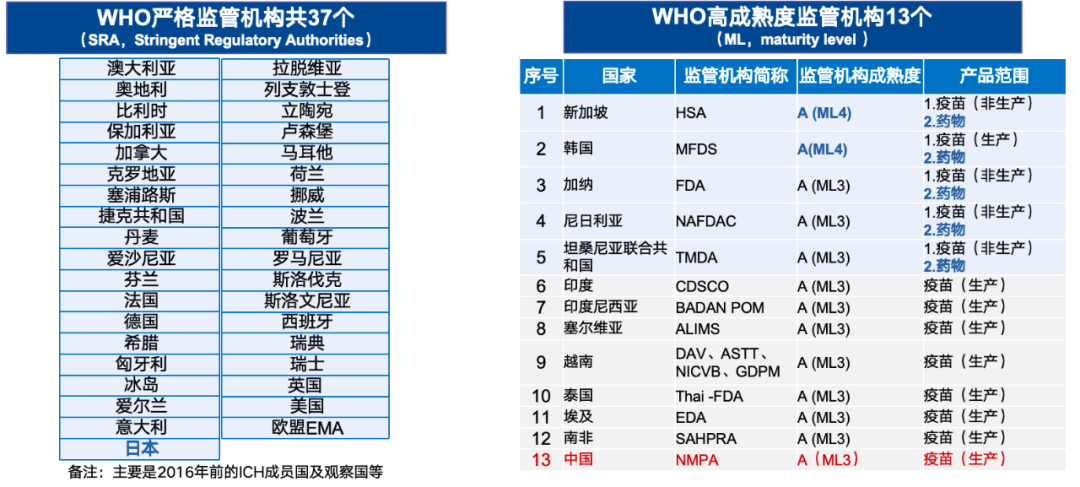
这意味着我国的整体监管能力已经达到一个新的台阶,在新的国际格局下,我们既要重视美欧日市场,也要关注广大发展中国家特别是“一带一路”国家的市场需求,为建立人类健康共同体做出应有贡献。然而当前我国监管机构的国际化认证水平依然有待加强,药品监管体系尚未进入WHO认证的严格监管机构和高成熟度监管机构,这导致我国药品出口面临巨大阻碍。未来,仍需不断强化高效能监管,进一步推动医药监管合作,建立科学高效权威的药品监管体系,在国际上积极开展药品监管建设性互信对话,深化高效、深层次合作,让创新成果早日惠及各国人民。
持续深化审评审批制度改革紧跟医药创新步伐。作为中国药品审批审评制度改革的起点,2015年国务院印发的《关于改革药品医疗器械审评审批制度的意见》所提出的调整收费政策目标在于提升药品审批的能力、人力和总体建设,通过药监局发布的《2022年度药品审评报告》的数据保守计算2022年企业缴费金额超过15.88亿元,但是CDE的年度财政拨款仅有3.32亿元。对此宋会长建议进一步调整优化审评收支制度,使得审评机构能够通过招募高水平的审批人员进一步加强审评队伍建设,与蒸蒸日上的医药创新相匹配。
医保和医疗:解放思想,以医保为抓手提升医药创新水平
宋会长表示面对老龄化人口的飞速增长,中国必须建立起医保、医疗、医药协同发展的综合体系,以面对我国患者日益增长的临床需求,但当前三医协同依然面临诸多挑战。如医院的合理用药问题,不仅造成医保基金不合理支出的增加,同时在肿瘤领域用药不合理反过来导致中国广大的患者资源无法有效转化为受试者资源,对创新研发产生“增本降效”的作用。据统计医保基金累计结存5年增长120%的情况下,医保基金对谈判药品支出占比不超过5%,而在销售端辅助用药份额高达16.9%,创新药仅占11%。尽管医保局面对创新药准入难题开通“双通道”政策,但中国处方外流比例发展至2022年仅有20%左右,远低于美、日等国家,使得“双通道”政策难以真正提升患者可及性。同时鉴于我国的医疗体系以公立医院为主,致使纳入医保几乎成为医院准入的必要条件。宋会长表示我国的基本医保制度是在中国仿制药的用药基础上建立,随着我国医药创新的发展,在仿制药“用的起”和创新药“用的上”需实现平衡,对于仿制药应保持“用得起”,对于创新药如果继续仅追求“用得起”反而会出现“用不上”,与设立医保的初衷背道而驰。对此宋会长建议解放思想,以医保支付为核心推动行业整体发展。比如对于加速通道上市的创新药,可以向企业提出可以借鉴国际上已有的经验,跟随式创新药(ME-TOO)上市第一年自动纳入医保目录,按照医保内同适应症最优疗法的标准予以支付,同时要求企业与该最优疗法开展头对头临床试验,第二年根据临床试验证据调整支付标准;对于证明优效的,提高支付标准;对于非劣效的按照原有标准,对于劣效的调出目录。“所以我们医保除了有降价机制,必须建立一个溢价机制,对于那些优效的产品要敢于提高支付标准。”
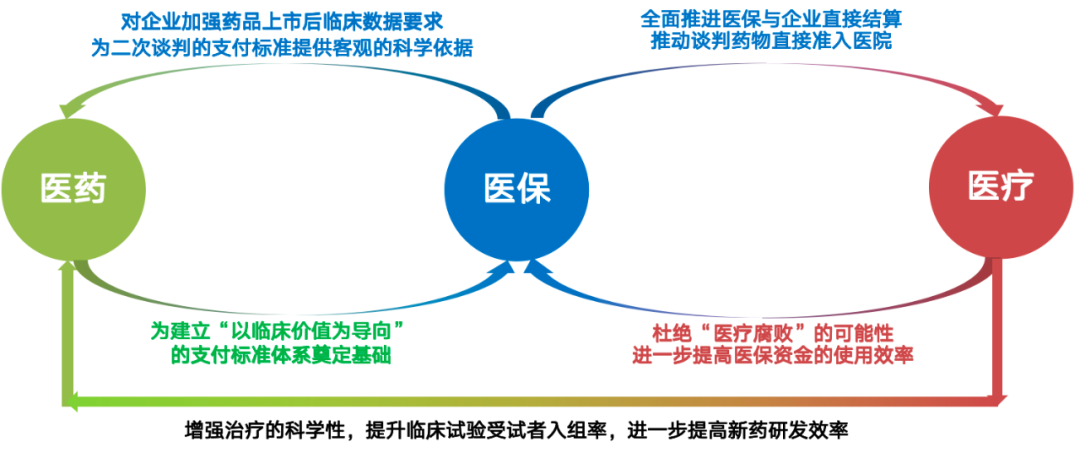
同时宋会长建议探索建立创新药专有管理目录(如丙类目录),对于创新药依据临床价值与医保支付能力弹性制定支付比例,同时为低收入人群单独提升支付比例。对于低收入人口,2023年国务院发布的《关于加强低收入人口动态监测做好分层分类社会救助工作的意见》已经明晰界定范围。
源头创新是三医协同发展的基石
宋会长表示,当前同质化研发现象凸显的主要原因是源头创新的缺失,临床角度几乎没有参与药物临床前研发,当下药物研发更多是“盯着药”而非“盯着病”。尽管我国从政策上已经开始关注转化医学,但是我国没有研究性医院,更缺少在医疗、基础研究与产业之间建立“产学研”的无缝对接。宋会长认为高风险的转化医学研究需要政府资金的支持。“对于风险过高,社会资本不愿介入的,政府资金应当补足。公用事业就是个体公司不愿意投入却又必须要做的工作,如修桥修路、改善环境等。”同时宋会长以新加坡科技研究局(A*Star)的运作模式举例,强调政府资金对于转化医学的重要性。
宋会长强调推动源头创新更需斩断医院和医生身上的枷锁。一方面建议研究者发起的临床研究(简称IIT研究)在风险可控的情况下有序放开,并以CAR-T为例说明IIT研究对我国医药创新发展的重要性;另一方面建议放开临床研究和产业资本之间的通道,首先需要把临床研究机构放到科研体系中,“我们一发转化政策文件,讲的都是高校和科研机构,很少谈到临床研究机构”,同时建议允许医生和企业或资本建立市场化的合作机制。
结语
最后宋会长强调医药行业的发展在产业政策支撑的同时,更需要市场政策的引领和保障,否则无法形成闭环。“国家无法让每一个企业都活得好,你活得好与不好,生与死是市场决定。但是,我们要通过建立公平、公正的市场为行业发展助力信心,就让那些真正做好药,高价值的企业能发展壮大。”

 产业资讯
产业资讯
 村夫日记LatitudeHealth
村夫日记LatitudeHealth  2024-12-21
2024-12-21
 47
47

 产业资讯
产业资讯
 动脉网
动脉网  2024-12-21
2024-12-21
 59
59

 产业资讯
产业资讯
 医药魔方Info
医药魔方Info  2024-12-21
2024-12-21
 51
51