 产业资讯
产业资讯
 Insight数据库
Insight数据库  2020-09-15
2020-09-15
 4950
4950
9 月 14 日,CDE 公示拟将苏州爱美津制药 4 类仿制药「麦格司他胶囊」纳入优先审评审批。该药是一款罕见病治疗药物,用于成人及儿童 C 型尼曼匹克病患者的进行性神经症状的治疗。
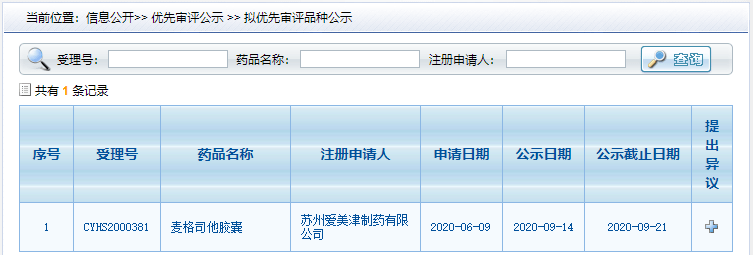
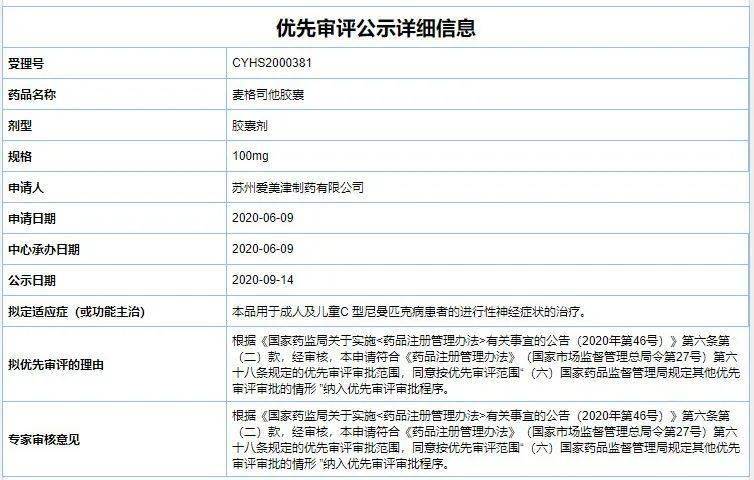
麦格司他是一种葡萄糖神经酰胺合成酶抑制剂,最早由西安杨森旗下瑞士爱可泰隆公司开发,用于 C 型尼曼匹克病的治疗。该产品于 2006 年获 EMA 孤儿药认证,2009 年在欧洲获批上市,商品名为 ZAVESCA,随后相继在 30 多个国家获批,是全球唯一批准用于 C 型尼曼匹克病的药物。
2015 年,爱可泰隆公司在国内提交麦格司他胶囊的上市申请,2016 年 11 月,经 NMPA 批准在国内上市,商品名为「泽维可」。2019 年的医保谈判中,包括麦格司他在内的 7 种罕见病用药谈判成功进入医保乙类目录,降价 10.4% 为 128 元(100mg/片),有效期由 2020 年 1 月 1 日至 2021 年 12 月 31 日。
C 型尼曼匹克病是一种罕见的常染色体隐性遗传的溶酶体贮积症,以神经系统症状为主要表现。该病多在晚婴期(2~6 岁)和少年期(6~15 岁)发病,症状恶化速度快,严重影响患儿生长发育,使其患者多在 10-25 岁死亡。此次仿制药拟纳入优先审评审批,或将加速仿制药上市,为相关患者提供新选择。

 产业资讯
产业资讯
 药时空
药时空  2026-01-23
2026-01-23
 31
31

 产业资讯
产业资讯
 药视声Medispace
药视声Medispace  2026-01-23
2026-01-23
 29
29

 产业资讯
产业资讯
 E药经理人
E药经理人  2026-01-23
2026-01-23
 30
30