 产业资讯
产业资讯
 丁香园Insight数据库
丁香园Insight数据库  2025-12-30
2025-12-30
 192
192
根据 Insight 数据库和 FDA官网,2025 年 FDA 药品评价与研究中心(CDER)共批准了 45 款新药,包括 33 款化药和 12 款生物制品。生物制品评价和研究中心(CBER)批准了 4 款 CGT 疗法、4 款疫苗和 3 款血液制品。(截至 2025 年 12 月 28 日,文末有完整表格和下载)
与往年相比,今年 CDER 批准的新药虽然数量略有减少,但创新含量极高,first-in-class 产品占比超过 50%。同时,药物类型也非常丰富,涉及 siRNA、ASO、ADC、双抗、多肽、非降解型分子胶、非抗体类融合蛋白等等。
今年,CDER 采用了多种方式加速新药审评,批准的新药中,有 19 款获得了 FDA 授予的突破性治疗资格,22 款获得了优先审评资格,15 款获得了快速通道资格,还有 11 款通过加速批准上市(注:部分产品同时获得上述资格,不去重)。这里面,宗艾替尼(勃林格殷格翰)还获得了局长国家优先审查券(CNPV)。
根据 Insight 数据库,CDER 批准的 45 款新药中,有 10 款已经在中国上市,其中阿夫凯泰(赛诺菲拥有大中华区权益)在中国首批,三天后才在美国获批,勃林格殷格翰的那米司特在中美两国同步获批。另外,还有 12 款处于申报上市的关键阶段,这再次说明中国的上市节奏和审评效率正在与国际全面接轨。
两款国产新药成功登陆美国市场
今年,有 2 款国产新药获 FDA 批准上市,分别是舒沃替尼和派安普利单抗。目前在美国获批的国产新药已经超过 10 款。
舒沃替尼是迪哲医药开发的一款口服、不可逆且针对多种 EGFR 突变亚型的高选择性 EGFR 酪氨酸激酶抑制剂(TKI),早在 2023 年 8 月就通过优先审评在国内获批上市。
2024 年 11 月,迪哲医药向 FDA 递交了该产品的上市申请。2025 年 7 月,舒沃替尼通过优先审评程序获 FDA 加速批准,用于治疗 EGFR exon20ins NSCLC。
舒沃替尼项目时间表

来源:Insight 数据库
派安普利单抗是正大天晴与康方生物合作开发的一款采用 IgG1 亚型并进行 Fc 段改造的新型差异化 PD-1 单抗,2025 年 4 月斩获 FDA 批准,用于一线治疗转移性鼻咽癌、单药用以铂类为基础的化疗治疗失败的转移性鼻咽癌。这是继特瑞普利单抗、替雷利珠单抗后,第 3 款在美国上市的国产 PD1 单抗。
自 2021 年 8 月首次上市以来,派安普利单抗已在国内获批用于多个癌种,包括经典型霍奇金淋巴瘤、鳞状非小细胞肺癌、鼻咽癌和肝癌。除肝癌外,其他适应症均已被纳入国家医保目录。
跨国药企依旧是获批主力军
从公司来看,跨国药企依旧是今年 FDA 新药获批的绝对主力军。其中 GSK 和阿斯利康表现尤为亮眼,凭借 3 款新药,在一众竞争者中脱颖而出,成为今年新药审批最大的赢家。
GSK 获批的新药分别是德莫奇单抗、吉泊达星和五价脑膜炎球菌 ABCYW 疫苗。其中德莫奇单抗是新一代超长效 IL-5 抗体,今年 12 月中旬获 FDA 批准上市,作为嗜酸性粒细胞表型重度哮喘患者的附加维持治疗药物,用于 12 岁及以上的成人和青少年患者。与美泊利珠单抗(每月一次)相比,德莫奇单抗具有更长的半衰期,仅需每半年注射一次。
阿斯利康获批的新药分别是 Zoliflodacin(II型拓扑异构酶抑制剂)、Brensocatib(DPP-1 抑制剂)和德达博妥单抗(TROP2 ADC)。其中德达博妥单抗是阿斯利康与第一三共合作开发的第 2 款上市 ADC 新药。今年 1 月,该产品在美国获批用于 HR 阳性、HER2 阴性乳腺癌,6 月拓展新适应症,用于非小细胞肺癌。
此外,诺华、拜耳、赛诺菲、辉瑞、勃林格殷格翰、艾伯维、第一三共也分别有 2 款新药斩获 FDA 批准。
本文限于篇幅,不一一赘述。想要了解更多新药情况,可前往丁香园 Insight 数据库查看,或添加小音下载表格,具体见文末。
2025 年 FDA 批准新药
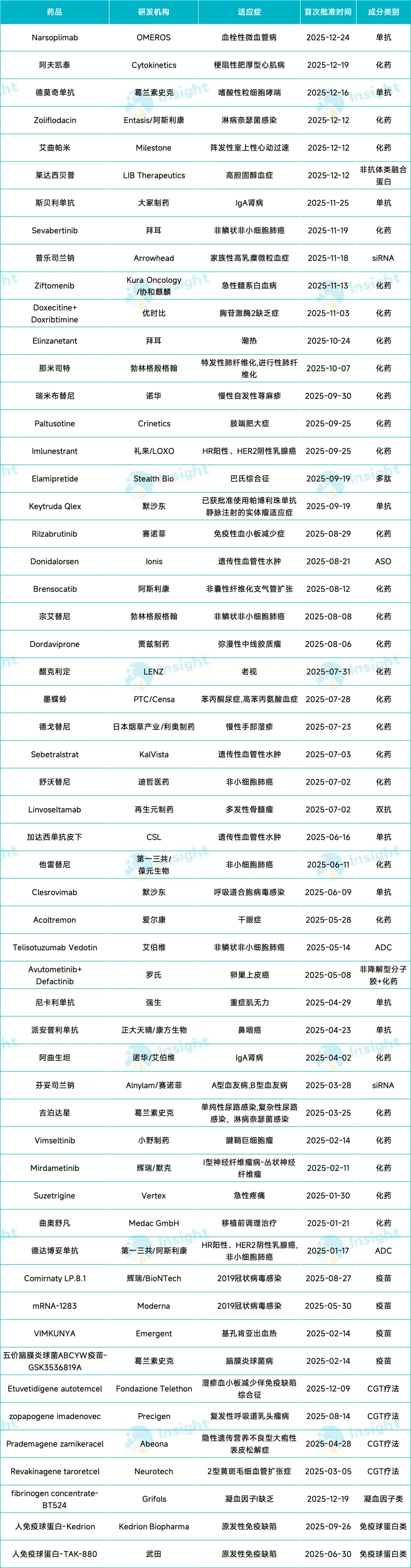
注:1.研发机构仅统计拥有美国权益的公司;2.数据截至 2025 年 12 月 26 日
丁香园 Insight 数据库整理了 2025 年 FDA 批准新药信息,扫描下方二维码添加小音,回复关键词 FDA新药 即可免费获取。

 产业资讯
产业资讯
 识林
识林  2026-01-19
2026-01-19
 25
25

 产业资讯
产业资讯
 识林
识林  2026-01-19
2026-01-19
 27
27

 产业资讯
产业资讯
 生物制药小编
生物制药小编  2026-01-19
2026-01-19
 26
26